<span id="9mlez"><optgroup id="9mlez"></optgroup></span>
近日,中國(guó)科學(xué)院合肥物質(zhì)院健康所谷紅倉(cāng)、張帆基因組學(xué)團(tuán)隊(duì)通過(guò)多組學(xué)綜合分析,揭示了一個(gè)新的lncRNA-mRNA/蛋白質(zhì)-代謝物網(wǎng)絡(luò),在結(jié)直腸癌(CRC)進(jìn)展和免疫調(diào)節(jié)中發(fā)揮著關(guān)鍵作用,為提高治療效果提供了有前景的治療靶點(diǎn)。該研究在癌癥研究經(jīng)典期刊Molecular Cance上發(fā)表。
結(jié)直腸癌表現(xiàn)出顯著的遺傳與表觀遺傳異質(zhì)性特征,這使得開(kāi)發(fā)新型治療靶點(diǎn)成為迫切需求。盡管免疫療法在癌癥治療中取得了顯著進(jìn)展,但約85%的結(jié)直腸癌患者因個(gè)體間遺傳及表觀遺傳特征的差異,表現(xiàn)出對(duì)治療的耐藥性。多組學(xué)研究方法通過(guò)系統(tǒng)整合基因組學(xué)、蛋白質(zhì)組學(xué)與代謝組學(xué)的多層次數(shù)據(jù),已成為解析疾病發(fā)病機(jī)制的重要技術(shù)手段。
研究團(tuán)隊(duì)針對(duì)結(jié)直腸癌組織及其配對(duì)正常鄰近組織,系統(tǒng)整合分析了轉(zhuǎn)錄組學(xué)、蛋白質(zhì)組學(xué)和代謝組學(xué)數(shù)據(jù),發(fā)現(xiàn)了差異表達(dá)的1394個(gè)長(zhǎng)非編碼RNA(lncRNA)、2788個(gè)mRNA、548個(gè)蛋白質(zhì)和91個(gè)代謝物。通過(guò)進(jìn)一步研究,識(shí)別出了一個(gè)顯著的相互作用網(wǎng)絡(luò),包括22個(gè)lncRNAs、14個(gè)mRNAs/蛋白質(zhì)和9個(gè)代謝物,其中,lncRNA 60967.1在該網(wǎng)絡(luò)中起關(guān)鍵調(diào)控作用。
功能驗(yàn)證顯示,lncRNA 60967.1在CRC細(xì)胞系和患者組織中顯著下調(diào),lncRNA 60967.1的過(guò)表達(dá)恢復(fù)了腫瘤抑制基因PLCD4的表達(dá),并提高了全反式視黃酸(ATRA)的水平。這一調(diào)節(jié)增強(qiáng)了IFN-γ誘導(dǎo)的凋亡,并增加了IFN-γ受體亞單位IFNGR1的表達(dá),從而部分逆轉(zhuǎn)了IFN-γ抗性。在小鼠模型中,lncRNA 60967.1的過(guò)表達(dá)促進(jìn)了免疫細(xì)胞的浸潤(rùn),并與抗PD-1治療協(xié)同抑制了腫瘤生長(zhǎng)。
通過(guò)轉(zhuǎn)錄組學(xué)、蛋白質(zhì)組學(xué)和代謝組學(xué)等多組學(xué)數(shù)據(jù)的分析,本研究識(shí)別出了一個(gè)涉及lncRNA、PLCD4、ATRA和PD-L1的CRC新型調(diào)控網(wǎng)絡(luò)。lncRNA 60967.1-PLCD4-ATRA軸在免疫反應(yīng)和腫瘤進(jìn)展的調(diào)節(jié)中起到了重要作用。該發(fā)現(xiàn)具有臨床意義:一方面為改善結(jié)直腸癌治療效果提供了潛在干預(yù)靶點(diǎn),尤其針對(duì)當(dāng)前治療耐藥的患者群體;另一方面,該調(diào)控軸可能作為評(píng)估治療反應(yīng)的生物標(biāo)志物,為個(gè)體化治療策略的制定提供新依據(jù)。后續(xù)研究將重點(diǎn)探索該調(diào)控網(wǎng)絡(luò)在臨床轉(zhuǎn)化中的具體應(yīng)用價(jià)值。
中國(guó)科學(xué)院合肥物質(zhì)院研究員谷紅倉(cāng)、研究員張帆、博士后趙寧寧和浙江大學(xué)邵逸夫醫(yī)院戴勝醫(yī)生為該論文的并列通訊作者。該項(xiàng)研究得到了國(guó)家科技重大專(zhuān)項(xiàng)、國(guó)家自然科學(xué)基金、中國(guó)科學(xué)院上海應(yīng)用物理研究所種子基金、浙江省重點(diǎn)研發(fā)計(jì)劃、2023年省部共建重點(diǎn)項(xiàng)目的支持。
文章鏈接:https://link.springer.com/article/10.1186/s12943-025-02359-x
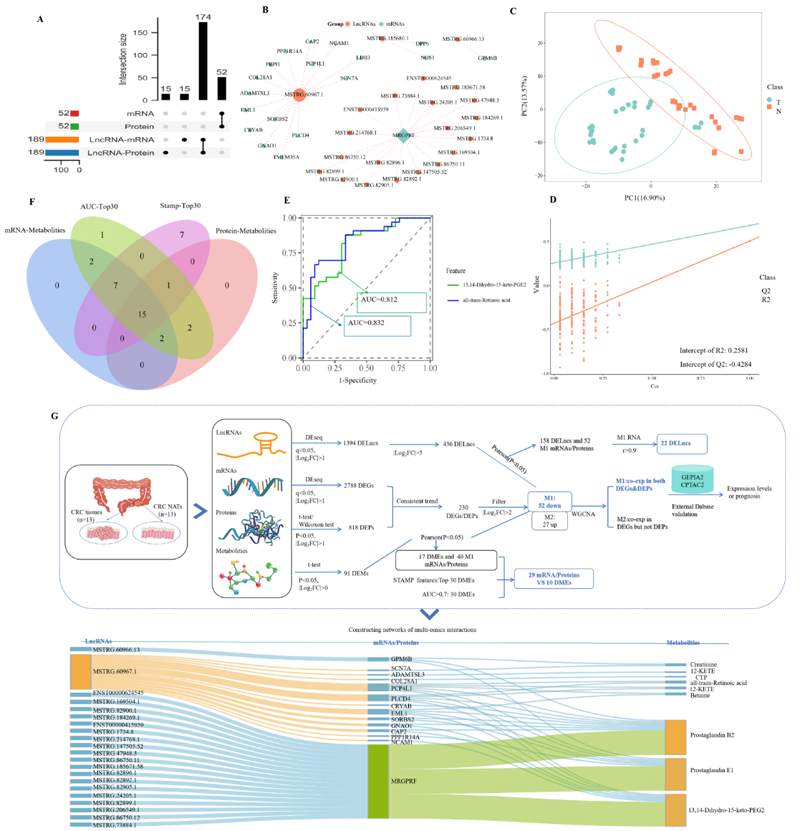
綜合多組學(xué)分析揭示了lncRNA、mRNA、蛋白質(zhì)和代謝物之間的網(wǎng)絡(luò)關(guān)聯(lián)
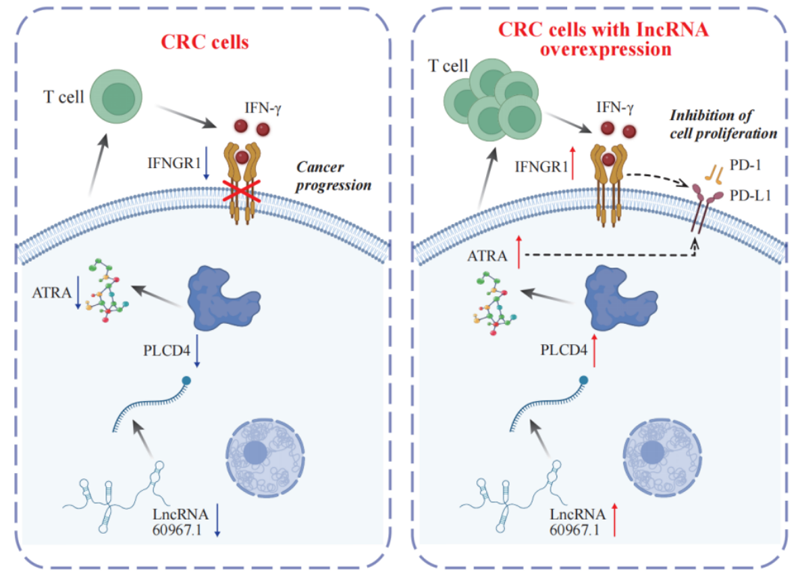
lncRNA 60967.1在調(diào)節(jié)PLCD4/ATRA軸及抗PD-1治療中發(fā)揮重要作用,調(diào)控免疫反應(yīng)并影響結(jié)直腸癌(CRC)進(jìn)展的模式圖
