<span id="9mlez"><optgroup id="9mlez"></optgroup></span>
近日,中科院合肥研究院劉青松研究員課題組和劉靜研究員課題組在針對FLT3-ITD突變選擇性的激酶小分子抑制劑研究方面取得新進展,發現了成藥性良好的第三代抑制劑CHMFL-FLT3-362。目前該成果在線發表于國際學術期刊Haematologica。
急性髓性白血病(AML)是由于髓性細胞通過克隆、增殖、異常分化等方式快速滲透至骨髓,血液和其他組織(脾、淋巴結、肝臟等)而引起的造血系統異常的癌癥,是成年人最常見的急性白血病,其發病率隨年齡增加,且病人生存率較低。研究表明,30%的AML與FLT3激酶突變相關。目前已有若干個FLT3激酶抑制劑被批準用于治療FLT3-ITD陽性的AML,但這些小分子抑制劑均對野生型FLT3和cKIT激酶具有強烈的抑制作用,在臨床上會導致骨髓抑制毒性,并能引發毛發白化病等副作用。正常的野生型FLT3激酶主要在人的骨髓細胞、早期祖細胞、樹突狀細胞祖細胞和CD34+的造血干細胞中表達,在造血干細胞和祖細胞的增殖和分化中起著重要的作用。因此,為了避免抑制正常野生型FLT3及cKIT激酶所帶來的不良影響,開發選擇性針對FLT3-ITD突變的小分子抑制劑具有重要的臨床價值。
在前期研究中,研究團隊已針對FLT3-ITD陽性的急性白血病開發了一系列具有自主知識產權的小分子抑制劑,包括第一代高選擇性的FLT3激酶抑制劑HYML-122(目前處于臨床I期)、第二代能夠克服多種耐藥突變的II型激酶抑制劑CHMFL-FLT3-213,以及首個第三代針對FLT3-ITD突變的抑制劑CHMFL-FLT3-335。為了進一步提高其活性、選擇性及成藥性,研究團隊利用計算機輔助藥物設計的方法,通過結構優化發展了新型第三代抑制劑CHMFL-FLT3-362。
在蛋白、細胞、動物層次上的研究表明,CHMFL-FLT3-362除了進一步提高了在FLT3-ITD與wt-FLT3等激酶間的選擇性之外,與已上市的FLT3抑制劑米哚妥林(Midostaurin)相比,能夠顯著降低斑馬魚模型的尾部畸形的出現。在連續給藥14天的小鼠模型實驗中,也沒有引起明顯的骨髓抑制毒性。這些實驗結果進一步驗證了FLT3-ITD突變選擇性的小分子抑制劑在臨床應用上可能具有更好的安全性。此外,CHMFL-FLT3-362在SD大鼠、KM小鼠及Beagle犬中表現出良好的藥物代謝動力學性質。在動物體內藥效評價方面,在MV4-11細胞皮下移植瘤的小鼠模型上,CHMFL-FLT3-362在150 mg/kg/day的劑量下的抑瘤率(TGI)高達95%,并且在MV4-11細胞原位瘤的小鼠模型上能夠顯著延長動物的生存時間。
該研究成果獲得了國家自然科學基金、中科院“個性化藥物”先導專項、中科院青促會、博士后基金特別資助等項目的支持。
文章鏈接:http://www.haematologica.org/content/early/2020/04/16/haematol.2019.244186.full.pdf+html
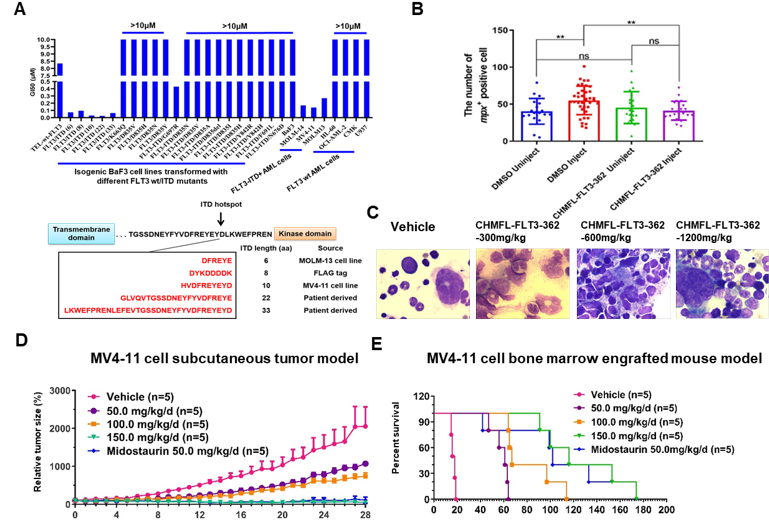
CHMFL-FLT3-362的作用機制及藥效數據
