<span id="9mlez"><optgroup id="9mlez"></optgroup></span>
近日,強磁場中心張鈉研究員課題組首次運用核磁共振(NMR)技術(shù)解析由端粒DNA序列d(G2T4G4T4G4)與短鏈d(TG4A)探針形成的分子間V-形G-四鏈體復合物結(jié)構(gòu),發(fā)現(xiàn)新型短鏈DNA探針能夠特異性識別包含V-shape關(guān)鍵堿基序列的端粒DNA,具有潛在抗癌前景。該研究成果在線發(fā)表于國際期刊Nucleic Acids Research(doi:10.1093/nar/gky1167)。
端粒DNA形成G-四鏈體結(jié)構(gòu)與抑制癌癥密切相關(guān),是優(yōu)良抗癌靶點。G-四鏈體中除了經(jīng)典的連接環(huán)區(qū)域外,還存在獨特的V-形支架結(jié)構(gòu)域,其不包含任何中間殘基,卻可以跨越三個G-四分體平面。這種V-形支架可以使兩個相鄰堿基之間糖磷骨架鏈的方向發(fā)生急劇逆轉(zhuǎn),同時又參與形成G-四分體核心的氫鍵連接。這些特性使得這種V-形支架本身與眾不同,因此本質(zhì)上作為藥物設(shè)計靶標時更容易被特異性識別。端粒DNA由重復堿基序列單元構(gòu)成,這就造成其被傳統(tǒng)反義互補鏈探針識別時,通常選擇性不理想。對此,張鈉課題組預測作為傳統(tǒng)反義互補鏈的替代方法,由兩個不同的DNA寡聚體能夠形成分子間的G-四鏈體,其中較長的DNA寡聚體作為靶標被短的富含G的DNA探針片段捕獲,進而有助于更特異性識別端粒DNA中富含連續(xù)G序列的重復結(jié)構(gòu)基序。然而,此前這種由不同長度的DNA寡聚體組成的分子間V-形G-四鏈體結(jié)構(gòu)尚未有報道。
在本項工作中,研究人員首先對尖毛蟲的端粒序列d(G2T4G4T4G4)和探針d(TGGGGA)形成的復合物進行了液體核磁共振結(jié)構(gòu)解析,證明該復合物是一種新型非對稱分子間V-形G-四鏈體。通過核磁共振的競爭結(jié)合實驗,發(fā)現(xiàn)采用該構(gòu)型與常規(guī)的G-四鏈體構(gòu)型相比熱力學更加穩(wěn)定且動力學形成速度快。后續(xù)研究人員進一步通過對原始序列進行堿基突變處理,證明在人源端粒DNA的天然突變體中,只要具備d(G2NG3NG4)特征的序列,明顯比其他序列更容易被探針識別和捕獲,從而為抗癌靶標端粒DNA區(qū)域的靶向探針設(shè)計提供了一種新的思路和理論支持。
該研究工作由論文第一作者博士后萬嬋娟,以及博士研究生付文強、景海濤,通訊作者張鈉研究員等人共同完成。該研究獲得了國家自然科學基金青年科學基金,國家自然科學基金聯(lián)合基金,國家重點研發(fā)計劃項目等多個項目的支持。核磁共振部分工作在穩(wěn)態(tài)強磁場實驗裝置上開展實施。
文章鏈接:https://academic.oup.com/nar/advance-article/doi/10.1093/nar/gky1167/5184730。
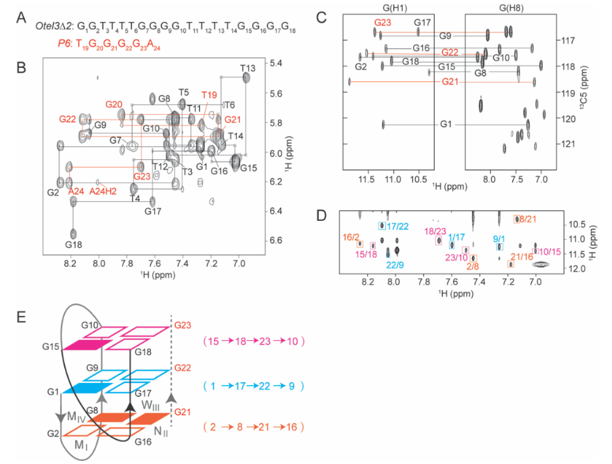
d(G2T4G4T4G4)與 d(TG4A)形成V-形G-四鏈體復合物的相關(guān)NMR實驗
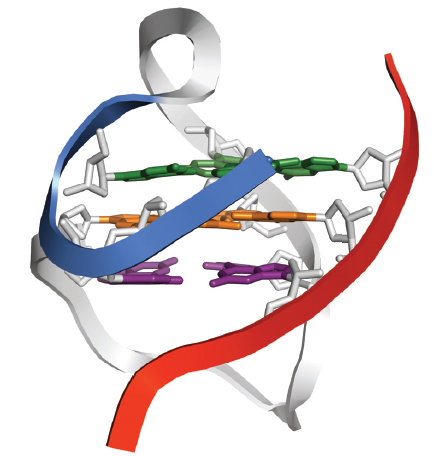
V-形G-四鏈體DNA復合物結(jié)構(gòu)三維模型(PDB: 6A7Y)
